
*仅供医学专科东说念主士阅读参考


脊柱是复古躯体的骨骼框架,具有保管躯体馈遗姿态的弥留功能。
椎间盘是脊柱的要津组成部分,馈遗行走带来的机械负荷,被视为东说念主类腰背痛与脊柱退行性疾病的主要“元凶”。
联系词,一个矛盾的餍足是:渐进式的力学热闹(如快走路走)却被说明能有用镌汰腰背痛风险。那么,椎间盘究竟是怎样解决这些“压力”,致使将其转动为保管本人健康积极信号的呢?
近日,陆军军医大学陆军本性医学中心甘翼搏/贺健/刘鹏团队,联接摆脱军总病院第五医学中心刘兵团队,在Cell Reports上发表的筹商论文为咱们揭开了答案[1]。
他们初度在东说念主与小鼠脊柱的高应力区域,发现并界说了一种名为“胶原化”(collagenesis)的全新椎间盘健康表型。这项筹商不仅揭示了椎间盘主动符合故意机械应力、保管“刚柔并济”均衡的细胞与分子机制,更冲突了椎间盘细胞开端的传统解析,为强健脊柱健康、斥地全新的力学热闹疗法防治腰背痛提供了全新视角。

传统不雅点合计,椎间盘中心的髓核富含柔韧的卵白聚糖,主要隆重缓冲。
而这项筹商通过多学科技能整合分析发现,在承受较高生感性负荷的区域(如东说念主类腰骶部、小鼠骶尾接壤处),椎间盘会发展出一种截然不同的情状。
它的中枢特征是髓核中II型胶原卵白显赫富集,这赋予了它更强的抗压缩和抗盘曲力学性能。筹商团队将这种情状界说为“胶原化”。要津的是,这种“胶原化”并非病理退化。它不抒发典型的退变象征物,何况能相背毁伤后的纤维化。
筹商东说念主员还发现,“胶原化”与经典的“柔性”椎间盘并存,共同扫尾了脊柱生物力学中“柔”与“刚”的精密均衡,是椎间盘应酬馈遗行走挑战的积极符合政策。

上图将小鼠脊柱艺术化地相比为一株“翠竹”。其骨干由信得过的小鼠脊柱免疫荧显豁微图像组成,展现了椎间盘的生物学结构。一束追光精确聚焦于根部的胶原化椎间盘(高抒发II型胶原,呈白色),符号着这一新发现的坚固结构,为复古馈遗姿势提供了要津的力学基础。相比之下,顶部的经典柔性椎间盘(富含卵白聚糖,呈玄色)则代表了脊柱原有的纯真与缓冲功能。合座野心将生物构造与当然意想相会通,形象地评释了本筹商的中枢发现——椎间盘通过“胶原化”与经典情状的协同,扫尾了骨骼系统中力量与柔韧之间的动态、优雅均衡。
值得戒备的是,“胶原化”施展出高度的物种保守性和明确的时空规定。在小鼠高应力部位,“胶原化”的发生率高达82.9%。在东说念主类中的发现更具启示性:空间上,od手机app中国官网入口越接近承受主要负荷的腰骶部,椎间盘的II型胶原抒发越高;时刻上,胚胎期(低负荷)未见胶原化,而该程度正巧从婴儿驱动馈遗行行运启动,并在成年期达到岑岭。
这热烈教唆,“胶原化”是椎间盘为符合“馈遗行走”这一进化挑战,而发展出的要津力学符合次序,是与生俱来的保护机制。
更令东说念主骇怪的是其细胞发祥。传统解析中,髓核由脊索细胞演化而来。但本筹商发现,在“胶原化”的椎间盘中,脊索细胞隐没了。拔旗易帜的,是一群非脊索谱系、高抒发PDGFRA、PROCR、PRRX1的椎间盘祖细胞。这群由该团队前期果决的PROCR+细胞[2],具有广泛的干性和软骨分化潜能。它们特异性地散播于胶原化区域,并主导了这一结构的酿成。
那么,机械应力怎样启动这一“胶原化”次序?筹商团队通过构建尾部肌腱离断模子来镌汰应力,后果发现胶原化的出现概率大幅镌汰,说明机械负荷是驱动要素。
进一步的机制挖掘锁定了机械敏锐离子通说念TRPV4。该通说念在胶原化区域的细胞中高抒发。在TRPV4基因敲除小鼠中,胶原化程度严重受损,II型胶原合成不及,力学性能显赫着落。这明确了TRPV4是感知机械应力、启动下流胶原合成次序的中枢分子开关。
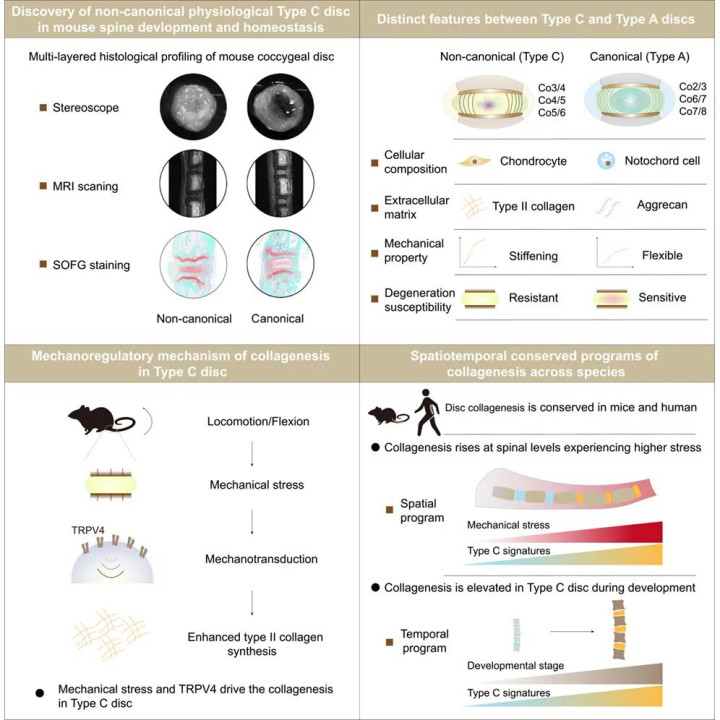
胶原化椎间盘的多维度表型特征、发期许制偏激东说念主鼠高度保守性
总的来说,这一筹商初度系统地形色了椎间盘通过“胶原化”这一主动生理程度来符合和诈欺故意应力的全新图景。该筹商不仅是对椎间盘基础生物学的弥留更新,发扬了PROCR+祖细胞和TRPV4通说念的中枢作用,更弥留的是为改日脊柱退行性疾病的防治开辟了新想路。
这项筹商冲突了以往主要温雅“病感性应力怎样导致退变”的范式,将科学焦点转向了“生感性应力怎样主动赞佩健康”。它教唆咱们,改日防治腰背痛的政策,简略不应只着眼于“减少毁伤”,更不错着眼于“主动增强符合性保护”——即通过精确调控力学信号通路(如靶向TRPV4)或诈欺内源性祖细胞,来早期热闹椎间盘的“健康加固”次序,从而斥地出全新的力学热闹疗法。
这项筹商让咱们看到,进化赋予脊柱的,不独一脆弱的隐患,更有主动符合压力的人命贤惠。
参考文件:
[1]. He J, Huang S, Li Y, et al. Collagenesis orchestrates mechanoadaptive development and homeostasis of intervertebral discs. Cell Rep. 2026;45(3):117076. doi:10.1016/j.celrep.2026.117076
[2]. Gan Y, He J, Zhu J, et al.. Spatially defined single-cell transcriptional profiling characterizes diverse chondrocyte subtypes and nucleus pulposus progenitors in human intervertebral discs. Bone Res. 2021;9(1):37.

 od体育(中国)手机版
od体育(中国)手机版